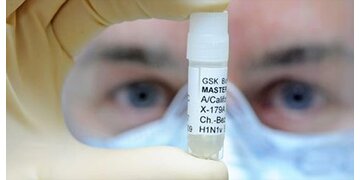
Schweinegrippe
Baxter startet Impfstoff-Studie
07.08.2009
Unklar ist, wann das Mittel an die Bevölkerung verabreicht wird.

Der Pharmakonzern Baxter will klinische Studien zur Bewertung der Sicherheit und Immunogenität des Impfstoffs Celvapan gegen die neue A(H1N1)-Influenza bei Erwachsenen, älteren Personen und Kindern noch im August beginnen. Die klinischen Studien werden ca. 1.000 Teilnehmer umfassen, die Beobachtungsstudie 9.000 Menschen, gab das Unternehmen bekannt. Wann der Impfstoff genehmigt und an die Bevölkerung verabreicht werden kann, steht noch nicht fest. "Wir möchten hinsichtlich des Zeitpunkts der Zulassung nicht spekulieren", so Baxter.
Bestellung liegt nicht vor
Österreich verfügt über einen
Vorvertrag mit dem Unternehmen über bis zu 16 Millionen Impfstoff-Dosen.
Eine Bestellung liegt laut dem Gesundheitsministerium noch nicht vor.
Der neue Impfstoff basiert auf einem mit einem anderen Virenstamm hergestellte Mock-up-Vakzine, daher ist auch ein vereinfachtes und schnelleres Zulassungsverfahren zulässig, bei dem Tests nicht vor sondern erst parallel zur Genehmigung durchgeführt werden könne. Die Basis, der Mock-up-Impfstoff, wurde weltweit bereits in fünf klinischen Studien mit mehr als 1.300 Teilnehmern geprüft, so Baxter. Zusätzlich wurden mehr als 3.500 Personen während einer fortlaufenden Phase-III-Studie geimpft.
Der Abschluss der klinischen Studien über Celvapan bilde laut aktuell geltender EU-Richtlinien und aufgrund der Dringlichkeit keine Voraussetzung für den Vertrieb oder die Lizenzierung des Impfstoffs, betonte der Konzern. Sobald mit nationalen Impfprogrammen begonnen wird, will Baxter mit einer umfangreiche Beobachtungsstudie starten.